Menu principal
- Accueil
- Le chirurgien
- Consultation
- Pathologies
- Vidéos
- Album photos
- FMC
- Questions internat
- Questions Résidanat
- Quoi de neuf ?
- Livres
- -- En cours de construction --
Pathologie fréquente dans notre pays : Goitre endémique, maladie de Basedow, et surtout nodule thyroïdien isolé qui pose un problème diagnostique.
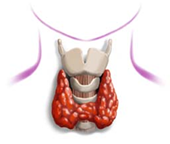
1 nodule sur 2 est découvert grâce à la palpation (systématique ou autopalpation).
Autres circonstances de découverte
– signes fonctionnels (dysthyroïdie, compression ou gêne cervicale, douleur d’apparition brutale)
– imagerie cervicale (Echographie, doppler ...)
La fréquence des nodules justifie la palpation systématique.
Le nodule thyroïdien se présente sous forme d’une hypertrophie arrondie, localisée cervicale antérieure, sous-hyoïdienne mobile à la déglutition.
Un nodule ≥ 1 cm est en principe palpable et doit être exploré
Nette prédominance chez la femme
– environ 4 femmes /1 homme, comme toutes les pathologies thyroïdiennes.
Les cancers thyroïdiens sont rares. 1,2 % de l’ensemble des cancers
Incidence annuelle faible : 2,5 / 100 000. Plus de 90 % des nodules explorés sont bénins. Des cancers occultes sont retrouvés dans 2 à 28 % des thyroïdes.
Pronostic des cancers thyroïdiens
Pour les formes nodulaires de cancer différencié le pronostic est en général bon. Pour une majorité des carcinomes papillaires et vésiculaires : survie à 5 ans > 90 %. Mais 5 à 10 % des nodules sont cancéreux. Le caractère malin doit être évoqué systématiquement. Le pronostic dépend du type histologique et du stade de prise en charge.
Bilan initial : l’examen clinique
ATCD personnels ou familiaux : Irradiation, nodule ou cancer thyroïdien, NEM2.
Caractéristiques du nodule :
– évolutivité à l’interrogatoire
– unique ou multiple, siège, consistance, dimension et contour
– sensibilité, mobilité
Signes de compression : dyspnée, dysphonie, dysphagie...
Signes de dysfonctionnement thyroïdien : hypo ou hyperthyroïdie
Signes évocateurs de carcinome médullaire : flush, diarrhée.
Examens biologiques :
dosage de la TSH systématique
TSH : en première intention, recherche d’une hypo ou hyperthyroïdie (TSH basse = nodule toxique ou prétoxique scintigraphie), ne renseigne pas sur le caractère bénin ou malin
Calcitonine : indications encore discutées
VS, ACE, thyroglobuline : pas d’indication de principe
Echographie thyroïdienne : Examen non invasif, largement disponible mais opérateur-dépendant.
Echographie thyroïdienne :
critères de qualité
-Appareil adapté / Opérateur entraîné,
-Sonde de haute fréquence, définition de l’ordre du mm
-peut être complétée par un Doppler couleur ou pulsé
Compte-rendu précis
– dimension, contours, échostructure de chaque lobe
– épaisseur de l’isthme
– description et caractéristiques échographiques du ou des nodules (échostructure, échogénicité, contours)
– adénopathies satellites
– compression ou déviation trachéale
Clichés avec repères ± schéma + conclusion non directive.
Cytoponction thyroïdienne
Examen ayant la meilleure valeur diagnostique de malignité
– si les critères de qualité sont respectés +++
– rapide, en ambulatoire, quasi-indolore
Contre-indications
– syndromes hémorragiques, anticoagulants
– « Non-indications »
– nodule chaud ou toxique
– nodule infra-centimétrique (hors cancer médullaire ou familial).
Limites de l’interprétation de la cytoponction thyroïdienne
Cytologie douteuse ou suspecte : 10 à 30%
– 15 à 30 % correspondent à un K vésiculaire
ou à une forme folliculaire d’un K papillaire
Cytologie non significative : 3 à 20%
– lésion maligne dans 10 % des cas
– à contrôler
Faux-négatifs : 5%
– erreurs d’interprétation (K papillaire non caractéristique)
– erreurs techniques.
Scintigraphie
Seuls les nodules froids sont suspects de cancers mais ils représentent 85 % des
nodules palpés.
Le caractère non fixant n'est donc pas suffisamment sensible pour donner des arguments en faveur de la malignité.
La scintigraphie est donc plutôt un examen réservé aux nodules avec TSH basse.
Nodules et cancers thyroïdiens
Le nodule thyroïdien se présente généralement sous forme d’une tuméfaction cervicale antérieure mobile à la déglutition avec le reste du corps thyroïde. Pathologie très fréquente : 4 à 5 % de la population générale présentent des nodules palpables cliniquement.
Les nodules infra-cliniques sont mis en évidence à l'échographie dans plus de 50 % de la population de plus de 60 ans. La fréquence des nodules augmente avec l'âge et les femmes sont plus touchées que les hommes.
La découverte d'un nodule thyroïdien pose la question du cancer thyroïdien, sachant qu'actuellement seuls 5 à 10 % des nodules opérés sont des cancers, la proportion étant beaucoup plus faible pour les nodules échographiques.
La découverte d'un nodule thyroïdien à l’examen clinique doit faire rechercher des arguments en faveur de la malignité.
Par l'interrogatoire et l'examen clinique
Terrain : jeune âge ou à l'opposé patients de plus de 60 ans avec un nodule isolé.
ATCD personnels d'irradiation du cou.
ATCD familiaux de cancers thyroïdiens qui font évoquer le carcinome médullaire et le syndrome de Sipple ou NEM2 (association cancer médullaire de la thyroïde, phéochromocytome, hyperparathyroïdie) mais il existe aussi des familles de cancer papillaires.
Signes cliniques locaux : nodule de plus de 3 cm, dur, douloureux, adhérent aux structures de voisinage, présence d'adénopathies cervicales, signes de compression ou d'irritation locale.
Signes cliniques généraux qui font rechercher un cancer médullaire : diarrhée motrice, flush.
l’examen clinique ne permet pas d’éliminer un cancer thyroïdien.
Par les examens complémentaires
Le dosage de la TSH permet de repérer les nodules toxiques ou prétoxiques (TSH
basse : nodule probablement chaud à vérifier en scintigraphie d'emblée, ce caractère fonctionnel avec extinction du parenchyme adjacent n'étant qu'exceptionnellement associé à un cancer). Dans les cancers thyroïdiens la TSH est généralement normale.
Le dosage de la calcitonine marqueur du cancer médullaire à demander en cas de symptôme et pour certains au moins 1 fois devant tout nodule. La place de cette exploration n’est pas encore consensuelle : son grand intérêt est qu’elle permet le diagnostic de tous les cancers médullaires.
Echographie cervicale :
Le nodule cancéreux est plus volontiers mal limité, hypoéchogène siège de petites calcifications mais aucun critère échographique n'est suffisamment fiable pour permettre un diagnostic de malignité.
L’échographie permet surtout la mesure exacte de la taille du nodule : indication chirurgicale pour les nodules solides de plus de 3 cm ; surveillance longitudinale pour les nodules plus petits,
Le diagnostic de kyste sur l’aspect liquidien,
Scintigraphie thyroïdienne : seuls les nodules froids sont suspects de cancers mais ne représentent que 85 % des nodules palpés. Le caractère non fixant n'est donc pas suffisamment spécifique pour donner des arguments en faveur de la malignité. La scintigraphie est donc plutôt un examen réservé aux nodules avec TSH basse.
L'examen clef est la ponction cytologique à l'aiguille fine.
On ponctionne les nodules palpables ou suspects en échographie, la limite est en général de 1 cm. La ponction permet d'analyser des cellules issues du nodule. Parfois elle permettra aussi d'évacuer un kyste.
4 types de résultats : bénin probable permettant de respecter le nodule, malin indiquant formellement la chirurgie, douteux notamment dans les lésions vésiculaires ou à cellules de Hurtle faisant discuter la chirurgie, ininterprétable nécessitant une nouvelle ponction.
Au total on peut proposer une stratégie diagnostique qui repose essentiellement sur la
cytoponction lorsque la TSH est normale.
Le traitement médical des nodules par hormones thyroïdiennes à dose frénatrice est peu efficace. Il peut être discuté à titre de test, son résultat ne constitue pas un argument permettant de réfuter le diagnostic de malignité.
Le traitement chirurgical consiste en une thyroïdectomie totale et examen anatomo-pathologique ou isthmolobectomie du côté du nodule avec examen extemporané.
Les cancers thyroïdiens
C'est un cancer rare, son incidence dans le registre des cancers de la thyroïde serait de 5 à 6/100 000/an chez la femme et de 1 à 1,5 /100 000/an chez l’homme.
Les cancers différenciés de la thyroïde
Ils se développent à partir de cellules thyroïdiennes vésiculaires ou thyréocytes.
Prédomine chez la femme jeune : âge moyen 45 ans, exceptionnel avant 10 ans.
Le cancer différencié représente 80 % et existe sous deux formes :
Conserve une structure vésiculaire. Malignité affirmée par le caractère invasif vis-à-vis de la capsule ou des vaisseaux thyroïdiens, ou par la présence de métastases : par voie hématogène (poumons, os cerveau), plus rarement par voie lymphatique (20 à 35% des patients).
Sur le plan clinique : Il s’agit le plus souvent d’un nodule palpable, indolore, peu évolutif, de consistance variable, généralement ferme.
Plus rarement le nodule est de consistance dure, irrégulier avec des adénopathie cervicale palpable, dysphonie (paralysie récurrentielle), voire une dysphagie.
• Sur le plan hormonal : il s’agit de patient en euthyroïdie clinique et biologique.
T TUMEUR
• Tx : tumeur non mesurée
• T0 : tumeur non accessible cliniquement
• T1 : tumeur de moins de 1 cm
• T2 : tumeur entre 1 et 4 cm
• T3 : tumeur de plus de 4 cm limitée à la thyroïde
• T4 : tumeur dépassant la capsule
Quand la classification repose sur l'anatomie pathologique la lettre p sera rajoutée.
N GANGLIONS
• Nx : ganglions non mis en évidence
• N0 : pas de ganglion
• N1 : métastases
M METASTASES
• M0 : absence de métastase
• M1 : métastases
Les facteurs pronostiques
La notion de facteur pronostique permet, pour un malade donné, d'évaluer la gravité de son cas et d'adapter la stratégie thérapeutique en fonction de cette gravité.
Les facteurs reconnus par la plupart des équipes sont :
• l'âge supérieur à 45 -50 ans
• la taille de la tumeur et notamment le stade T4
• le type histologique : cancers peu différenciés
• l'existence de métastase
Un score pronostique peut être établi pour chaque malade lors du diagnostic.
Le diagnostic
Les signes cliniques :
• Le plus souvent : nodule isolé (cancer dans moins de 10 % des nodules)
• Parfois signes évocateurs d'emblée : gêne cervicale, compression, douleur, nodule dur,
adénopathies cervicales, flush et diarrhées en rapport avec un cancer médullaire. Les
signes locaux sont particulièrement marqués dans les cancers anaplasiques. Ils sont par
contre fréquemment absents dans les cancers différenciés : l’examen clinique ne suffit
jamais à éliminer un cancer.
• Parfois, métastases révélatrices plutôt adénopathies cervicales pour les cancers
papillaires, métastases à distance pulmonaires et osseuses pour le cancer vésiculaire.
La stratégie diagnostique a été exposée dans le chapitre nodules : elle repose essentiellement
sur la cytoponction puis l’examen anatomopathologique des nodules déclarés suspects à la
cytoponction.
Le traitement des cancers thyroïdiens différenciés (Papillaire et vésiculaire)
La chirurgie
Les protocoles chirurgicaux sont variables et doivent être adaptés au score pronostique après un inventaire des lésions.
Le plus souvent, en cas de cancer clinique (lésion de plus de 1 cm) on pratique une
thyroïdectomie totale avec dissection des récurrents, ne laissant aucun résidu thyroïdien mais en protégeant les parathyroïdes en préservant leur vascularisation et un curage adapté.
Dans les microcancers < 1 cm souvent découverts fortuitement (leur pronostic est excellent et les récidives sont rares) sur l'examen anatomopathologique définitif, il est souvent possible de ne pas réopérer les patients, même si le geste pratiqué n'a été que partiel, mais avec une surveillance régulière.
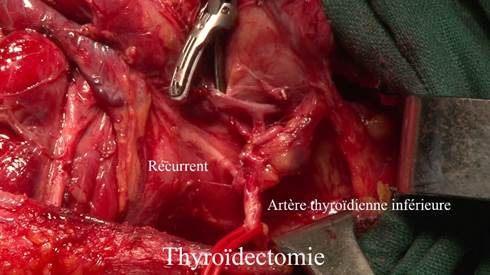
Dissection du nerf récurrent au cours d’une thyroïdectomie.
Dissection des pédicules vasculaires thyroïdiens.
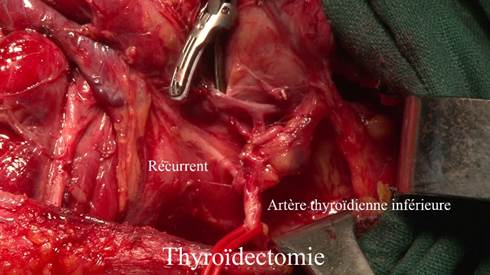
Thyroïdectomie : Section aux ciseaux ultrasoniques des branches de l’artère thyroïdienne inférieure
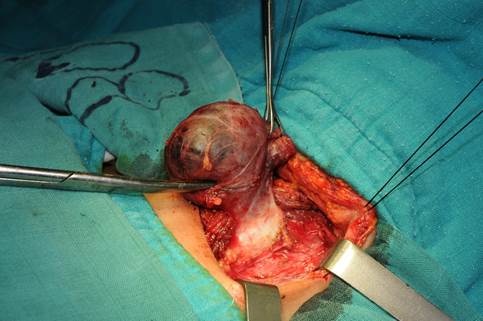
Section des ligaments de Gruber
Utilisation thérapeutique de l'I 131 après la chirurgie
L'I131 est un élément essentiel dans le traitement et la surveillance des cancers différenciés de la thyroïde à l'exclusion des autres cancers qui ne fixent pas l'iode. Cette méthode permet d'effectuer une radiothérapie métabolique ciblée sur les cellules thyroïdiennes. La captation de l’iode est fortement stimulée par la TSH : c’est pour cela que les traitements par l’iode 131 sont faits en hypothyroïdie. Après thyroïdectomie totale l'I131 permet l'ablation de tout le tissu thyroïdien cervical restant et le bilan des lésions à distance. Une fois la thyroïde entièrement détruite (préalable indispensable à son efficacité) l’iode 131 pourra être utilisé pour traiter les métastases.
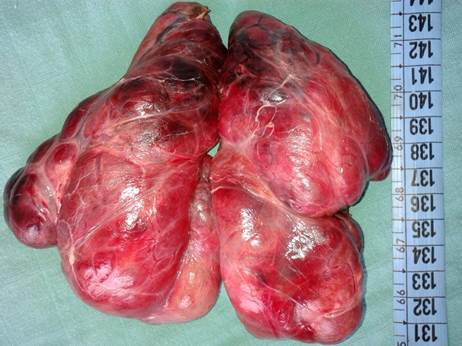
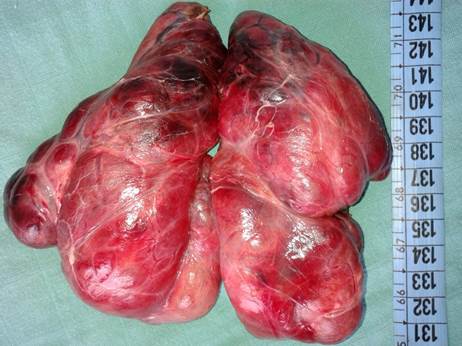
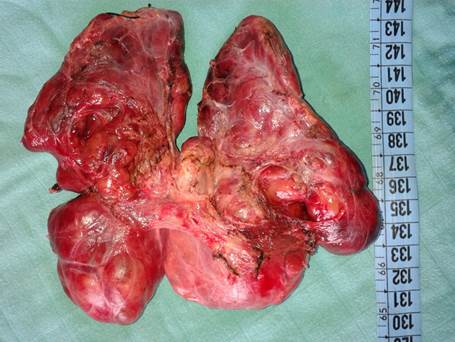
Pièce de thyroïdectomie totale pour goitre.
Préparation des malades
L'administration de l'I131 implique de mettre le patient en hypothyroïdie. L'élévation de la
TSH ainsi obtenue, stimule la captation de l'iode par les cellules thyroïdiennes (arrêt du
traitement de LT4 pendant 5 semaines, relais éventuel par la T3 dans les 15 premiers jours).
En s'assurant de l'absence de surcharge iodée (bétadine, cordarone, examens radiologiques avec produits de contraste iodé).
A l’avenir l’emploi de la TSH recombinante humaine (Thyrogen) permettra sans doute de
remplacer la mise en hypothyroidie des patients pour élévation de la TSH endogène. En 2005
l’emploi de la TSH recombinante est encore réservé au diagnostic de récidive.
L'hospitalisation en chambre protégée est obligatoire dès que la dose administrée est
supérieure à 740 MBq (20 mCi) pour recueil des effluents. L'iode radioactif (3,7 GBq = 100
mCi) est administré sous forme de gélule. Aucun effet secondaire n'est à redouter tant que les
doses cumulées restent faibles.
Détection scintigraphique
Systématique 4 jours après la prise d'iode. Elle permet d'évaluer l'importance du reliquat thyroïdien et d'effectuer un bilan des lésions à distance.
Le traitement freinateur
Il est systématique dans les cancers différenciés hormono-sensibles. Les cancers différenciés de la thyroïde sont sensibles à la TSH qui joue un rôle de facteur de croissance. La mise des patients sous thyroxine (le traitement freinateur) a pour but de prévenir ce risque en inhibant la sécrétion hypophysaire de TSH. Le caractère efficace du freinage est jugé sur le dosage de la TSH (< 0,2 μUI/ml) sans signe clinique d'hyperthyroïdie.
Les autres traitements
• L'irradiation externe : Utilisant les hautes énergies, l'irradiation peut être très utile :
- dans les formes extracapsulaires
- dans les métastases douloureuses
• La chimiothérapie : elle est peu ou pas efficace dans les cancers différenciés.
Surveillance des patients
La surveillance repose sur l'examen clinique (palpation de la région cervicale à la recherche d'une récidive locale et surtout d'adénopathie cervicale), le dosage de la thyroglobuline marqueur biologique du tissu thyroïdien, l'échographie cervicale, et la scintigraphie corps entier à l'iode 131.
Le dosage de la thyroglobuline
La thyroglobuline (Tg) est le marqueur tumoral des cancers différenciés de la thyroïde après
thyroïdectomie totale. En l'absence de tissu thyroïdien, son taux doit être indétectable. Toute élévation de ce taux indique la persistance d'un résidu tumoral. Le dosage de la Tg doit être couplé à la recherche d'auto-anticorps anti-thyroglobulinequi interfèrent dans le dosage de la Tg.
Le taux de Tg doit être vérifié après sensibilisation par la TSH obtenue par un arrêt du traitement frénateur(Arrêt de la thyroxine pendant 4 semaines entraînent une stimulation des cellules métastatiques) ou après injection de TSH recombinante (Thyrogen) ce qui évite de mettre le patient en hypothyroïdie.
Les scintigraphies corps entier à l'iode 131
Les scintigraphies dites diagnostiques, utilisant de petites doses d’Iode 131 (2 à 5 mCi) ne
montrent généralement aucune fixation si la thyroglobuline reste indétectable après stimulation par la TSH. Leur utilisation systématique est donc abandonnée. Par contre lorsque la thyroglobuline s’élève au dessus s’un certain seuil on recommande d’administrer de fortes doses d’Iode 131 (100mCi) après stimulation par la TSH (endogène, patient en hypothyroidie) ce qui a un intérêt diagnostique et éventuellement thérapeutique.
Les examens morphologiques
L'échographie cervicale : c'est l'examen majeur de surveillance quand du tissu thyroïdien a été laissé en place. Elle détecte les récidives locales et les adénopathies.
Le PET scan après injection Fluodesoxyglucose semble l’examen le plus sensible pour la
détection des métastases ne fixant pas l’iode 131.
Cette surveillance est maintenue à vie.
Les métastases
La fréquence des métastases varie de 10 à 20 % selon les séries.
La présence de métastases à distance dans les cancers différenciés de la thyroïde aggrave
considérablement le pronostic, puisque seulement 23 % des patients sont vivants à 10 ans, alors que le taux de survie à 10 ans, en l'absence de métastases varie de 78 à 98 % selon les études.
Elles sont découvertes dans la moitié des cas au moment du diagnostic.
Elles sont localisées par ordre de fréquence décroissante : aux poumons, à l'os, plus rarement métastases cérébrales, hépatiques, exceptionnellement cutanées.
11 % sont découvertes à un stade infra-radiologique.
Les cancers anaplasiques de la thyroïde
Développés à partir de la cellule vésiculaire, ils sont caractérisés par leur dédifférenciation et leur agressivité. 5 à 15 % des cancers thyroïdiens. Ils se voient généralement après 50 ans et représentent probablement l’évolution d’un cancer différencié non traité.
L'histologie est faite de cellules géantes, monstrueuses, envahissant et détruisant les structures thyroïdiennes normales. Elles ne produisent pas de Tg, ne fixent pas l’iode, n’expriment pas de récepteurs à la TSH.
Clinique
• La tumeur est manifeste, d'évolution rapide (quelques semaines) volumineuse (> à 3 cm)
adhérente aux plans profonds et superficiels, extrêmement dure, parfois inflammatoire.
• Une dysphonie, une gêne à la déglutition peuvent se manifester précocement.
• Des ganglions sont volontiers palpables.
Des signes généraux : asthénie, amaigrissement, anorexie, fébricule sont souvent présents.
Diagnostic
• La TSH est souvent normale, parfois légèrement élevée (hypothyroïdie par destruction du tissu normal).
• La cytologie signe le diagnostic, et permet le diagnostic différentiel avec les lymphomes et cancers secondaires.
• L'examen ORL, la radiographie pulmonaire et la TDM thoraco-cervicale précisent l’extension.
Evolution
• Spontanée : décès en quelques semaines ou mois, sur un mode essentiellement local
(Envahissement, compression, rupture des gros vaisseaux).
• La chirurgie complétée par un protocole de radiothérapie externe accélérée et une
chimiothérapie peuvent repousser l'échéance de quelques mois. L’évolution se fait
quand même vers le décès par récidive locale ou métastases à distance. La mise en
place d’une prothèse endotrachéale permet de lutter contre la compression trachéale
tumorale.
Le cancer médullaire de la thyroïde (CMT)
5 à 8 % des cancers de la thyroïde. Tumeur des cellules C (parafolliculaires) de la thyroïde qui sécrètent la calcitonine (CT). Il existe des formes sporadiques ou génétiques familiales (30% des CMT). Les formes familiales sont soit isolées (CMT familial isolé) soit associées à un syndrome de néoplasie endocrine multiple (NEM) de type 2 : NEM2A = CMT+
phéochromocytome +/- hyperparathyroïdie, NEM2B =CMT+neuromatose cutanéo-muqueuse et syndrome Marfanoide +/-phéochromocytome, +/-hyperparathyroïdie. Toutes les formes de CMT familial (isolé, 2A, 2B) sont dûes à la présence d’une mutation du gène RET. Mutation germinale dominante, qui peut se rechercher sur une simple prise de sang (ADN leucocytaire).
Le risque de transmission de la mutation à l’enfant est de 50%. Donc dans les formes
familiales de CMT : un dépistage très précoce est possible en identifiant les enfants qui ont
reçu la mutation de RET. Ces enfants auront un traitement préventif radical : thyroïdectomie
totale à une âge très jeune (3 ans généralement).
Histologie, caractère sécrétoire, évolution
Immunohistochimie positive pour la Calcitonine et l’ACE. Il peut y avoir sécrétion d’autres
hormones par la tumeur (ex : ACTH). Dans les formes sporadiques la tumeur est souvent
unique, dans les formes familiales elle est généralement bilatérale ou associée à une
hyperplasie des cellules C.
Le CMT se voit à tout âge, il est caractérisé par sa diffusion lymphophile extrêmement
précoce (métastases ganglionnaires cervicales présentes chez 90% des patients porteurs d’un
CMT clinique), et son potentiel métastatique à distance (foie, poumon, os). Il est de moins
bon pronostic que les cancers différenciés de la cellule vésiculaire, la survie globale à 10 ans
des patients traités est 70%.
Clinique
Le nodule thyroïdien, +/- adénopathies sont souvent les seules manifestations.
On peut retrouver des signes lié à une lésion de NEM 2 associé (ex phéochromocytome) ou à
une sécrétion endocrine par le CMT (troubles du transit (diarrhée), flushs, voire syndrome de
Cushing)).
Examens
TSH normale.
Au stade de nodule palpable la CT de base est en général très largement au dessus de la
normale (N<10 pg/ml) et elle est stimulable par la pentagastrine.
L’ACE est souvent élevé.
La scintigraphie retrouve un nodule froid.
La cytologie confirme le diagnostic mais elle peut être prise en défaut, elle est moins sensible
que le dosage de la CT.
Traitement
Chirurgie difficile réservée à des équipes expertes. Thyroïdectomie totale avec curage
ganglionnaire cervical extensif qui est impérativement bilatéral dans les formes familiales
(récurrentiel+jugulo-carotidien). Avant la chirurgie il faut avoir éliminé systématiquement un phéochromocytome qui sera éventuellement traité en premier.
L’iode 131 n’a évidemment aucune place dans le traitement des cancers médullaires de la
thyroïde (les cellules C ne captent pas l’iode)
Dépistage et prise en charge des CMT familiaux
Il est fondamental de rechercher une forme familiale devant tout CMT, même apparemment
isolé. Cette recherche doit comporter un examen clinique (syndrome Marfanoide, neuromatose, signes de phéochromocytome..) et un dosage de calcémie, PTH, dérivés methoxylés. Il faut établir un arbre généalogique et déterminer la CT de base et si possible sous stimulation par la pentagastrine chez les apparentés au 1er degré. L’avènement de la
génétique a simplifié ce dépistage : si une mutation de RET est identifiée chez un individu elle pourra être rapidement recherchée (Dans le sang périphérique) chez les autres membres de sa famille.
Les tumeurs rares de la thyroïde
Lymphomes
Soit lymphome primitif de la thyroïde soit localisation secondaire d’un lymphome généralisé.
2 à 3 % des tumeurs thyroïdiennes. La majorité des lymphomes primitifs se développent à partir d’une thyroïdite auto-immune (Thyroïdite de Hashimoto). Sujets âgés (souvent 70 ans), prédominance féminine 3/1.
Ils se présentent comme des nodules froids évolutifs avec parfois hypothyroïdie et signes
compressifs.
Le diagnostic repose sur l'étude immuno-histochimique (population monomorphe du clone
lymphocytaire responsable).
Le traitement et le pronostic sont celui du lymphome : traitement chirurgical réservé aux petites tumeurs, radiothérapie externe et chimiothérapie.
Conclusion
La prise en charge du cancer de la thyroïde est particulièrement bien codifiée. 2 groupes de patients s'opposent. Les plus nombreux ont un cancer thyroïdien bien différencié sans métastase, de bon pronostic. Quand cela est nécessaire, l'iode 131 permet un traitement spécifique in situ. Le traitement frénateur est un des éléments du contrôle à long terme.
Par contre, quelques patients ont un cancer peu différencié, qui fixe peu ou mal l'iode et dans ce groupe le cancer de la thyroïde demeure d'évolution redoutable.